APASL名家讲堂丨贾继东教授:慢加急性肝衰竭肝移植的理想时机
编者按
一、慢加急性肝衰竭的定义及流行病学
ACLF的定义
近年来,不同的国际协会均提出了ACLF的定义,但在慢性肝病基础、急性损伤病因和是否包括肝外器官衰竭等方面仍存在很大差异或争议[1],详见图1。
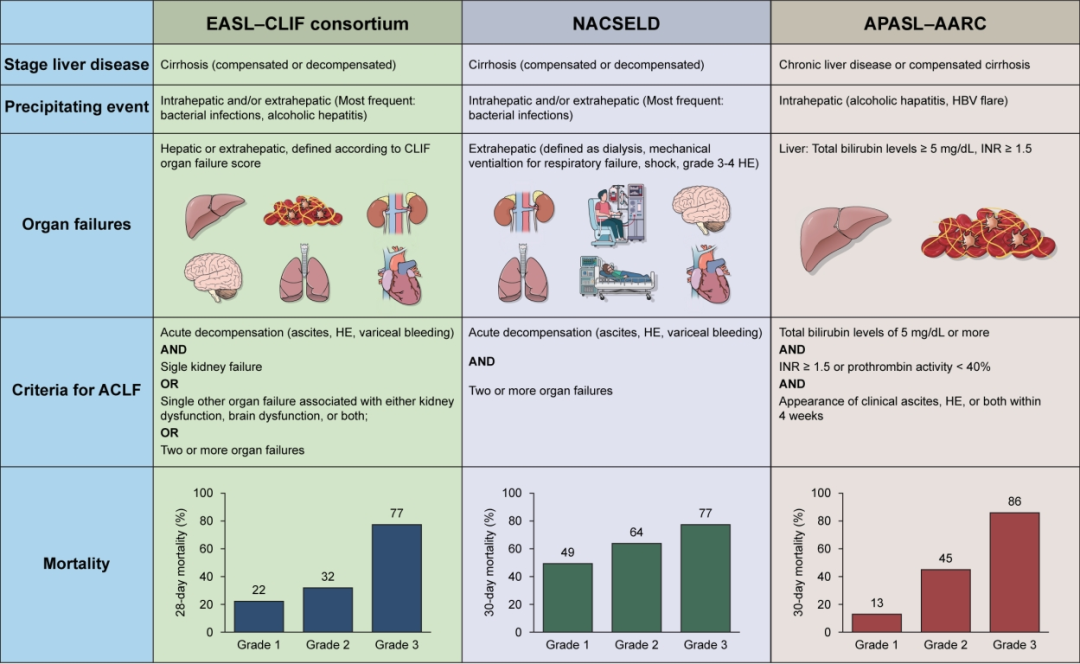
图1. 亚欧美三大肝病学会对ACLF的定义[1]
APASL共识
APASL于2009年首次发布了ACLF定义,并于2014年和2019年更新。最终将ACLF定义为:在已知或尚未发现的慢性肝病基础上,患者出现黄疸(TBil≥5 mg/dL)和(或)凝血功能障碍(INR≥1.5或PTA<40%)为最初临床表现的急性肝脏损伤,发病4周内合并腹水和/或肝性脑病(HE),同时伴有28 天的高病死率。由于亚太地区ACLF主要为嗜肝病毒(尤其为HBV)感染所致,ACLF的定义更侧重于肝脏衰竭本身,这有利于ACLF的早期诊治并防止向多器官功能衰竭发展。
欧洲肝脏研究学会(EASL)标准
EASL慢性肝衰竭联盟(EASL-CLIF)将ACLF定义为与肝内或肝外器官衰竭相关的肝硬化急性失代偿。器官衰竭评分纳入肝、肾、脑、凝血、循环和呼吸6大系统功能。根据器官衰竭的数量,ACLF患者按死亡风险分为ACLF 1-3级。在EASL-CLIF定义中,同时强调肝脏衰竭和肝外器官衰竭,把肝内和肝外因素都被认为是ACLF的诱因,其中最常见的是细菌感染和酒精性肝炎。
北美终末期肝病研究联盟(NACSELD)标准
NACSELD对ACLF的定义是基于507例急性失代偿期肝硬化伴发感染患者的观察数据,并于随后证实在非感染的肝硬化患者同样适用。NACSELD更强调肝外器官衰竭,最终将ACLF定义为至少存在2种严重的肝外器官衰竭,包括休克、3或4级HE、肾脏替代治疗或机械通气。
针对HBV相关ACLF(HBV-ACLF),2018年中国重型乙型肝炎研究小组(COSSH)在分析了我国13个中心的1322例患者的临床资料后,将其定义为:在HBV感染引起的慢性肝病(包括肝硬化和非肝硬化)基础上,表现为肝功能急性失代偿合并肝脏或肝外器官衰竭的一组具有短期高病死率的临床综合征。这是首个针对HBV-ACLF的定义。COSSH研究还建立了COSSH-ACLF评分系统,分别纳入了肝、肾、脑、凝血、循环、呼吸系统以及年龄等指标,并根据评分将HBV-ACLF分为3级。
(二)ACLF的流行病学
ACLF全球患病率和死亡率都很高。纳入43 206例ACLF(EASL-CLIF标准)患者的荟萃分析显示,失代偿期肝硬化患者ACLF的全球患病率为35%,南亚最高为65%。全球90天死亡率为58%,南美洲最高为 73%(图2);酒精(45%)是最常见的潜在慢性肝病病因,感染(35%)是最常见的ACLF的诱因(图3)[2]。
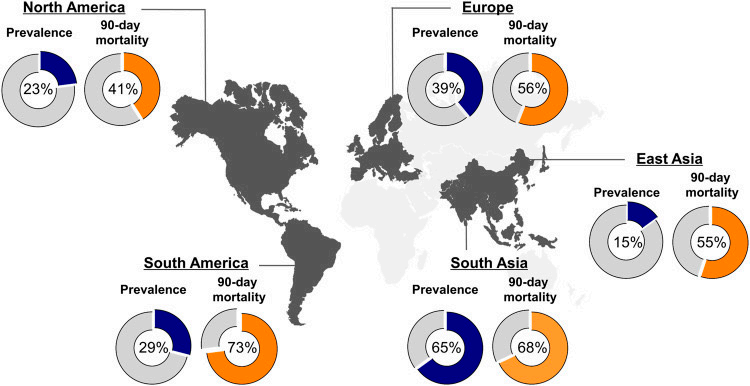
图2. ACLF 全球患病率和死亡率
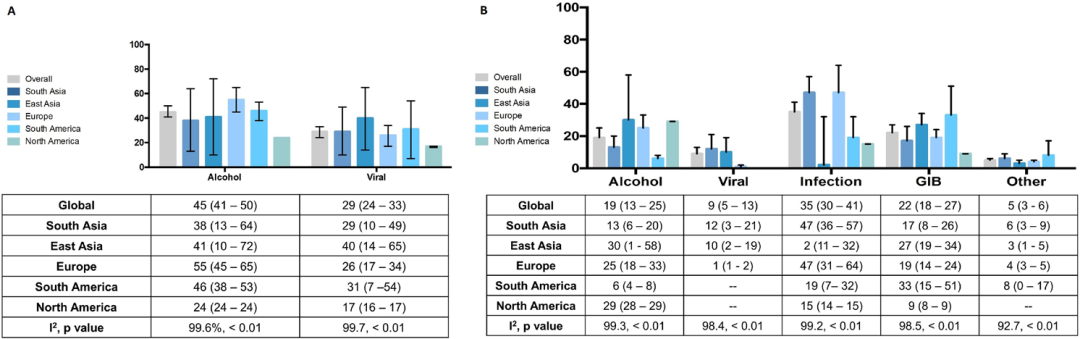
图3.全球潜在慢性肝病病因和ACLF诱因
二、慢加急性肝衰竭的预后评估
ACLF的临床特征
研究发现,ACLF病程可变,可在几天内改善或恶化,或病程稳定(图3D);因此,诊断时的预后评估不如3~7天后评估准确(图3E)[3]。
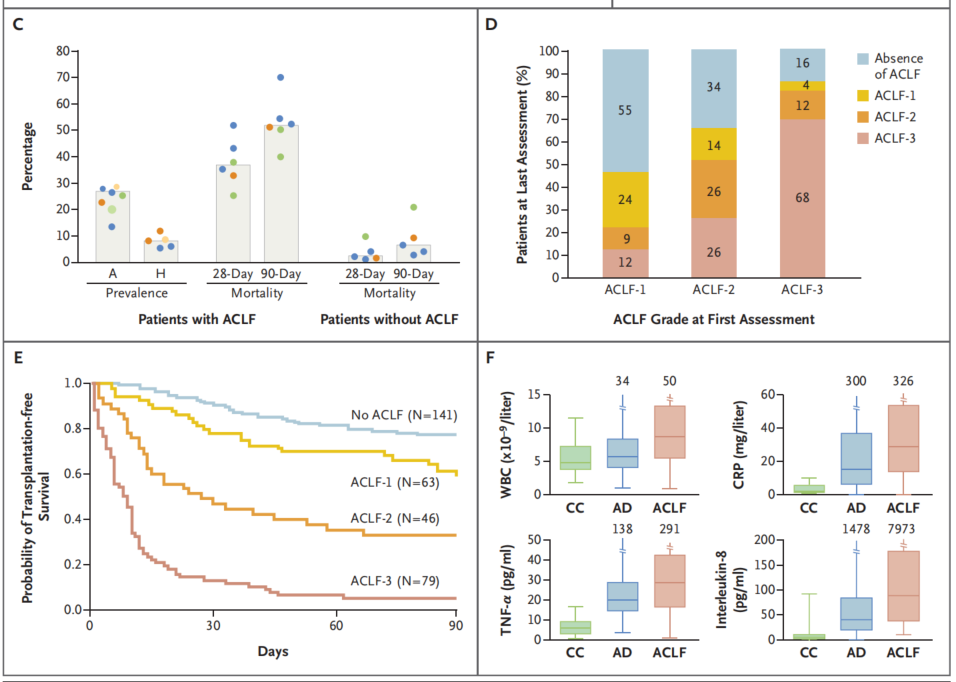
图3. ACLF患者的临床特征
COSSH-ACLF评分
ACLF患者短期病死率高,应用评分系统进行早期识别并治疗至关重要。目前常用的评分系统有CTP评分、MELD系列评分、CLIF-SOFA评分、COSSH-ACLF评分等。对于我国较常见的HBV-ACLF,最常用的评分系统为COSSH-ACLF,主要纳入PT-INR、年龄、血清胆红素水平,构建的评分公式能较为精准地预测预后。
COSSH研究[4]发现,无论是否存在肝硬化,HBV、TBil≥12 mg/dL 和 INR≥1.5的患者均应纳入 ACLF的诊断定义。根据EASL-ACLF标准,HBV病因患者诊断率只有22.5%,而COSSH-ACLF标准可以将41.8%的HBV病因患者诊断为ACLF,诊断率增加了近20%,从而增加了这部分患者及时进行强化治疗的机会(表1)。

基于研究发现和外部验证,COSSH-ACLF(0.741×INR+0.523×HBV-SOFA+0.026×年龄+0.003×TB)优于其他5项评分(图4)。
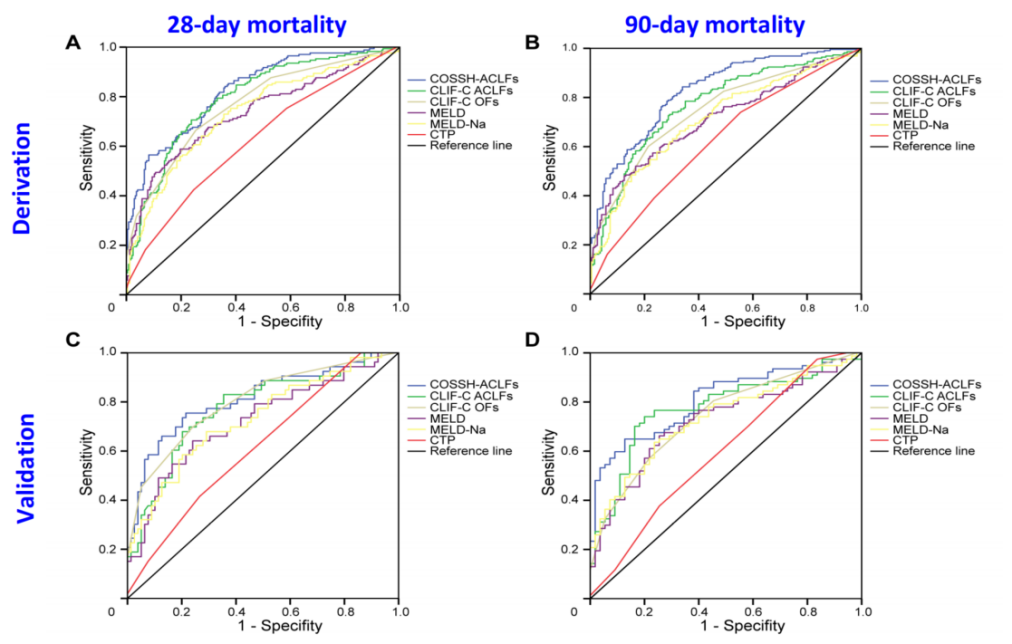
图4. 预后模型预测HBV-ACLF患者28天和90天死亡率的ROC
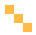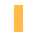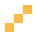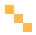
三、慢加急性肝衰竭的肝移植时机
对ACLF的病情有了精准全面的评估后,下一步便是明确肝移植的适应证及禁忌证,精准把握肝移植的手术指征,选择最合适的手术时机。根据《2019年亚太肝病学会共识建议:慢加急性肝衰竭管理更新》[5],早期肝移植可避免脓毒血症和多器官功能衰竭,ACLF患者在疾病早期就应进行肝移植评估(B1);但目前没有一个公认的标准和评分系统,能够早期、准确预测哪些ACLF患者能从肝移植中获益(A2)。
肝硬化或慢性肝病患者应抓住干预机会,避免进展为ACLF并改善预后。评估流程为:肝硬化或慢性肝病患者因诱发因素引起肝和肝外器官衰竭或出现ACLF,应进行容量复苏、处理感染、支持衰竭器官,并进入ICU管理评估、肝移植候选人评估,及早考虑肝移植的资质,评估是否应进行肝移植(图5)[6]。
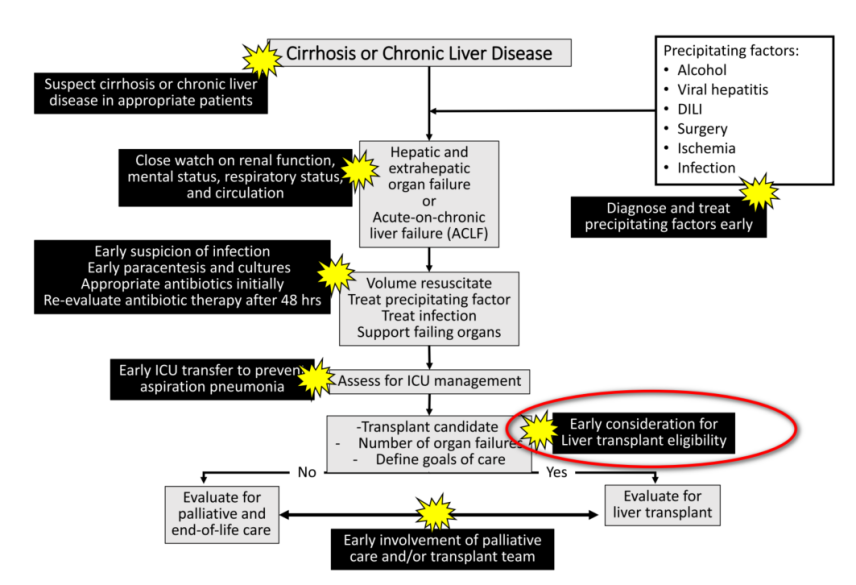
图5. 肝硬化或慢性肝病患者的评估流程
图6阐释了ACLF自然史以及肝移植治疗窗口期的概念,提示ACLF患者在脓毒症或多器官衰竭发生前行肝移植,有望获得良好预后,且风险可接受[7]。在中国的2项单中心研究中,ACLF患者肝移植后第1、3、5年的生存率分别为76%~72%、78%~74%[8]。
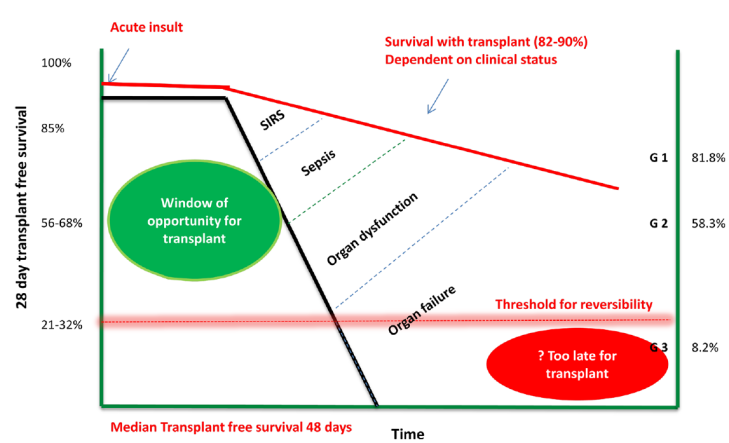
图6. ACLF自然史的图示(其中y轴代表28天时的无移植存活)
欧洲ELITA/EF-CLIF 合作研究(ECLIS)[9]表明,在欧洲,ACLF 2-3级患者进行肝移植的百分比有显著差异,等候名单的优先性应考虑ACLF 2-3级患者25%的死亡风险;欧洲ACLF患者肝移植后1年生存率>80%,且与ACLF分级无关(图7)。
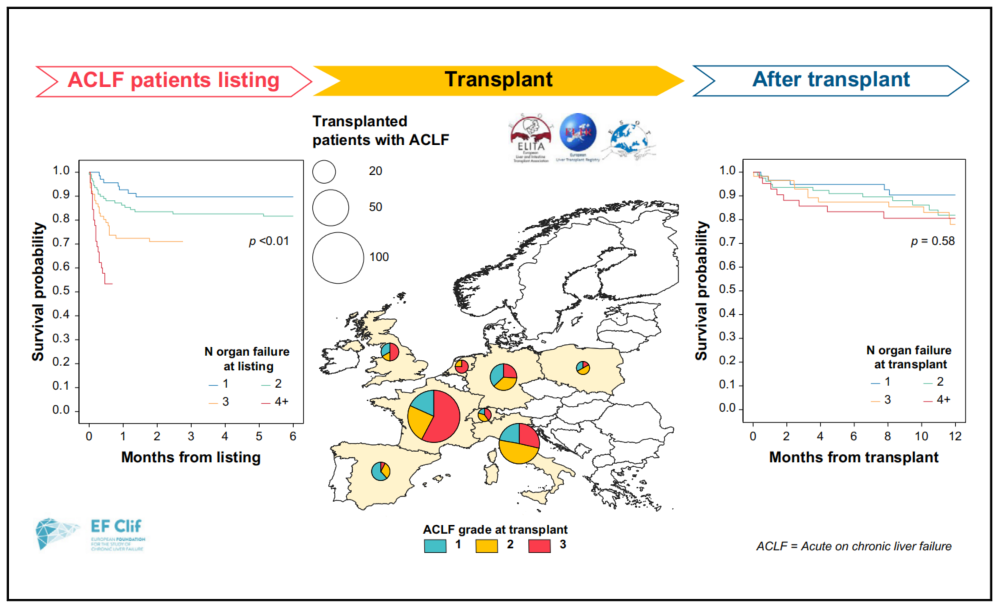
图7. 欧洲ELITA/EF-CLIF 合作研究图示
中国学者开展的一项回顾性队列研究[10]旨在比较EASL-CLIF和APASL-ACLF标准不同等级患者肝移植后的长期预后。分析显示,APASL和EASL-CLIF标准对于肝移植后患者的生存预后均有良好的区分能力(P=0.0065、P<0.0001,图8)。AARC-1级患者在肝移植后近2年的生存率接近AARC-0级患者;2年后的长期生存率有下降趋势,更接近AARC-2级患者。EASL-CLIF标准对于ACLF 1级和非ACLF患者之间的区分能力更好。ACLF 1和2级患者的生存率相似,且均显著高于ACLF 3级患者。
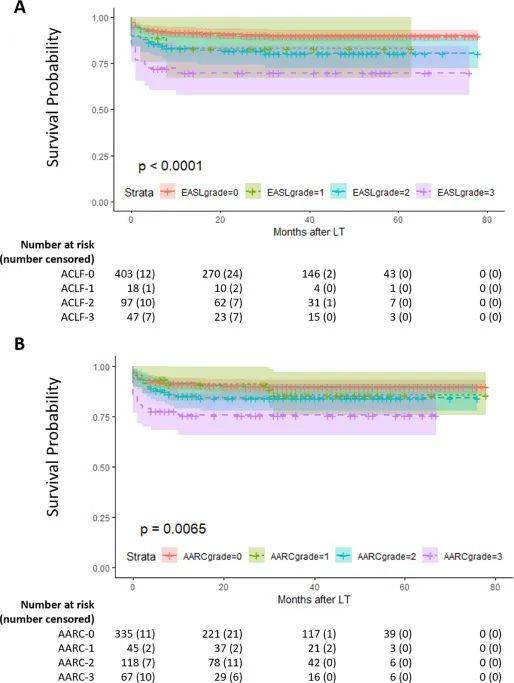
图8. 患者生存曲线
印度一项对218例ACLF患者的回顾性研究[11],旨在报告ACLF(EASL-CLIF)活体肝移植的预后与生存获益。研究显示,移植后1年生存率在不同级别的ACLF间具有可比性(92.9%、85.4%、75.6%;P=0.15,图9)。在ACLF 3级患者中,不能进行活体肝移植的患者90天存活率极低(5.9% vs.78%;P<0.001)。ACLF患者活体肝移植后生存率良好。
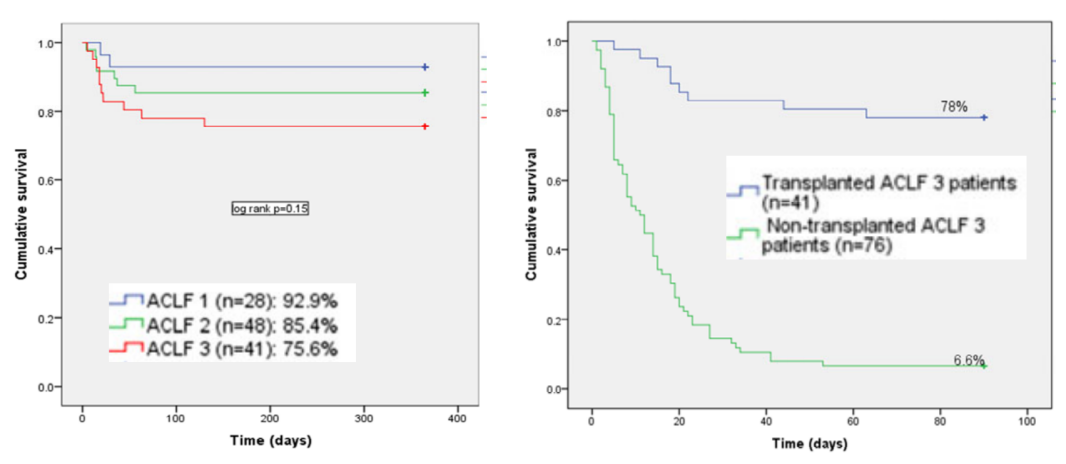
图9. 活体肝移植后累积生存率
日本一项回顾性研究[12]评估采用日本ACLF标准对ACLF和活体肝移植患者严重度分级的影响。结果显示,采用日本ACLF标准,对于诊断ACLF及其严重度特别是多器官衰竭的存在,即使在活体肝移植的情况下也会导致病死率,ACLF 3级患者活体肝移植并无获益(图10)。
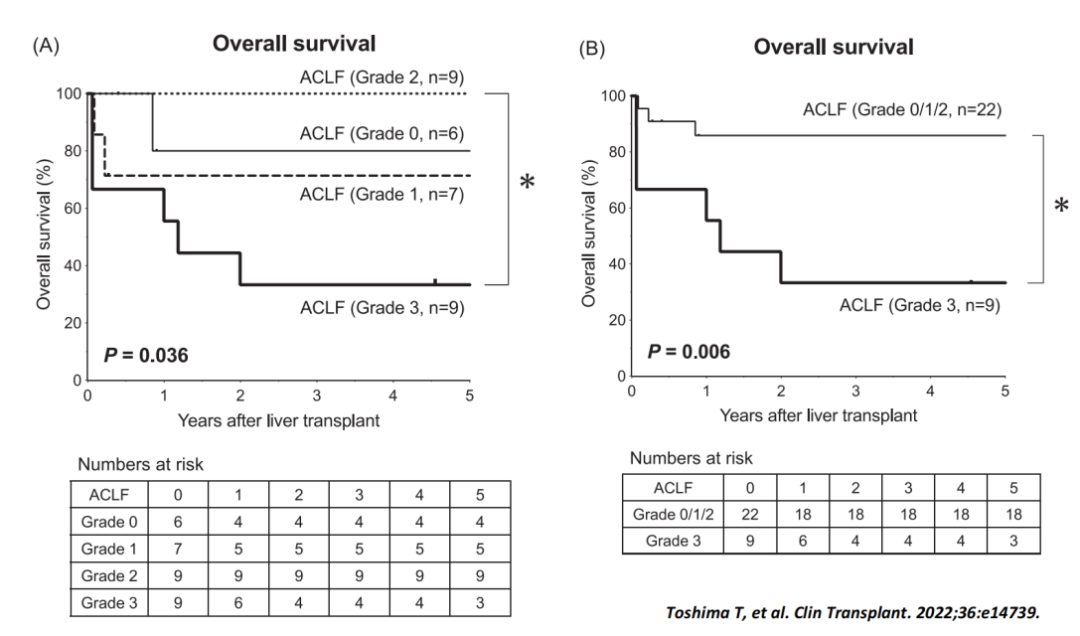
图10. 日本标准活体肝移植后累积生存率
ACLF 3级患者行肝移植存有争议。UNOS注册研究[13]显示,肝移植等待名单上的ACLF 3级患者,即使MELD-Na评分较低,其死亡率或名单移除率仍较高;而肝移植,特别是列入名单 30 天内进行的肝移植,可增加这部分患者生存率(图11)。
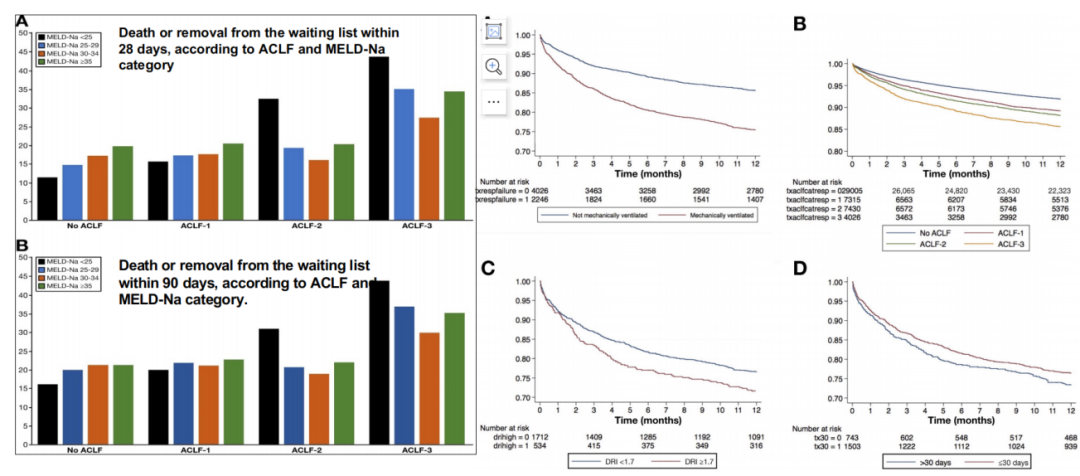
图11. 患者28天和90天内死亡或从等候名单中删除(左);患者生存曲线(右)
关于ACLF患者肝移植的最佳时机,虽然并没有定论,但似乎可以参考以下流程进行评估和判断[8]。首先,基于适当的标准进行ACLF的识别与风险分层,评估是否存在未控制的败血症、肝外恶性肿瘤、难治性胃肠道出血等情况,如果不存在,继续强化支持治疗4~7天,逆转器官衰竭,同时启动肝移植登记程序;对于ACLF 2或3级患者,如果不能恢复到0或1级,应进行紧急登记和加急肝移植手术(图12)。
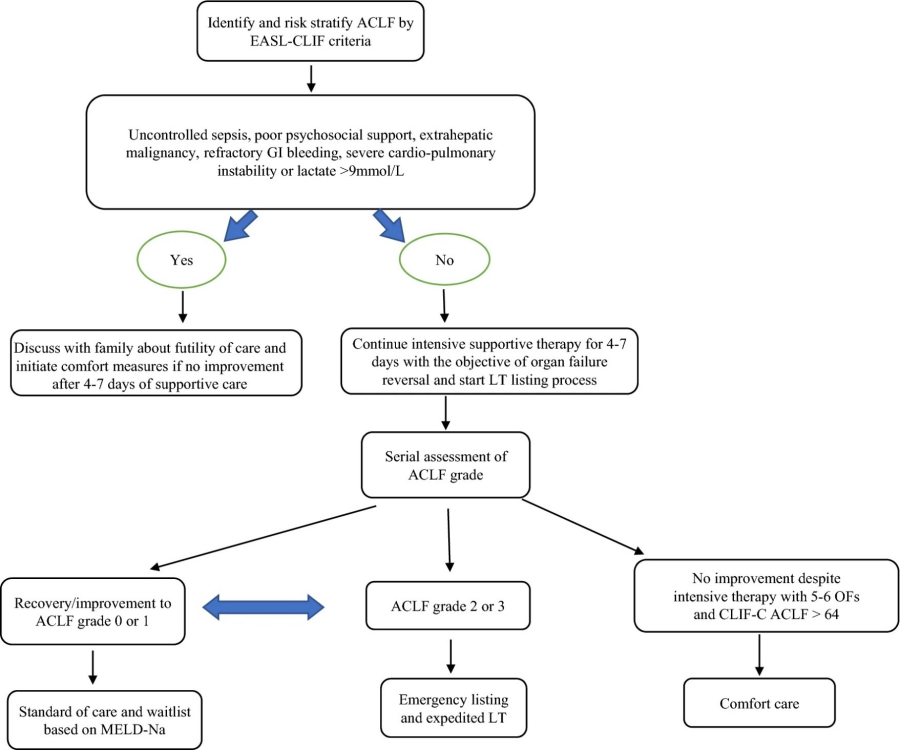
图12. ACLF患者肝移植的算法
小结
声明:本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。
(来源:《国际肝病》编辑部)
小提示:87%用户已下载掌上医讯App,更方便阅读和交流,请扫描二维码直接下载App

(本网站所有内容,凡注明来源为“掌上医讯”,版权均归掌上医讯所有,欢迎转载,转载请注明出处,否则将追究法律责任。凡是本网站注明来源为其他媒体的内容为转载,版权归原作者所有,转载仅作分享,文章观点不作为掌上医讯观点,如有侵权,请及时联系我们,联系电话:0532-67773733)

